- PORPHYRINES ET PORPHYRIES
- PORPHYRINES ET PORPHYRIESLes porphyrines sont des pigments d’un très grand intérêt biologique. Elles constituent une partie fonctionnellement essentielle de certaines macromolécules protéiniques indispensables aux processus d’oxydation. On retrouve en effet une porphyrine combinée au fer (l’hème): dans les hémoglobines et les myoglobines , transporteurs d’oxygène atmosphérique; dans la catalase et les peroxydases , capables de catalyser respectivement le transfert de l’oxygène moléculaire et celui de l’oxygène atomique détachés d’un substrat; dans les cytochromes , qui fonctionnent dans la chaîne respiratoire intracellulaire comme transporteurs d’électrons. Le groupement prosthétique de la chlorophylle et de la bactériochlorophylle, agents de la photosynthèse, est également une porphyrine renfermant un atome de magnésium. Dans la molécule de la vitamine B12 figure une porphyrine qui contient un atome de cobalt. Une porphyrine combinée au cuivre peut «activer» l’hydrogène et intervenir comme catalyseur dans les réactions d’hydrogénation. L’oxydation du tryptophane en formylcynurénine est sous la dépendance d’une enzyme héminique (porphyrinique), la tryptophane-pyrrolase . On trouve donc les composés porphyriniques, remplissant des fonctions physiologiques fondamentales, dans toutes les cellules vivantes, aussi bien végétales qu’animales. Aussi admet-on en général que les porphyrines constituent les premiers maillons de la chaîne évolutive qui, synthétisés dans des conditions terrestres primitives par voie abiogénétique (non enzymatique) à partir des composés organiques simples, ont rendu possibles la naissance et l’évolution des êtres vivants.Pour les biochimistes et pour les médecins, le rôle des porphyrines est d’une importance encore plus évidente en pathologie. Une série de maladies, réunies sous le terme de porphyries , sont caractérisées par la surproduction des porphyrines libres, non liées à un métal. D’autre part, les troubles métaboliques des porphyrines accompagnent un grand nombre d’affections diverses et leur étude facilite le diagnostic et l’analyse pathogénique de ces dernières. Il en est ainsi en particulier pour l’intoxication par le plomb, dont le dépistage, en médecine du travail, est réalisable grâce au dosage des porphyrines dans les urines.1. Les porphyrinesCaractères chimiquesLes porphyrines constituent une vaste famille. Toutes sont des pigments. Toutes présentent à l’état libre et en lumière ultra-violette une magnifique fluorescence rouge, nettement décelable dans une solution de porphyrine allant de 50 à 1 000 millionièmes, ce qui est un caractère analytique précieux.Toutes les porphyrines sont des dérivés tétrapyrroliques cycliques, dont les formules peuvent être ramenées à celle de la porphine , composé d’abord théorique, puis synthétisé par Hans Fischer. La porphine est formée de la réunion, en cycle fermé, de quatre noyaux de pyrrole, reliés par des ponts méthéniques (=CH 漣), numérotés par des lettres grecques. Deux des quatre azotes sont porteurs d’un atome d’hydrogène. Les carbones aux sommets (carbones pyrroliques), numérotés de 1 à 8, fixent chacun un atome d’hydrogène (fig. 1).La structure des diverses porphyrines dérive de celle de la porphine par remplacement des hydrogènes aux sommets par divers groupements fonctionnels. Ces remplacements sont réalisés, pour les porphyrines biologiquement les plus importantes, par quatre variétés de fonctions chimiques: méthyle (face=F0019 漣CH3), acétyle (face=F0019 漣CH2 漣COOH), propanoïque (face=F0019 漣CH2 漣CH2 漣COOH) et vinyle (face=F0019 漣CH=CH2). L’introduction de ces groupements fonctionnels dans la molécule de porphine rend plusieurs atomes de carbone de celle-ci asymétriques, d’où l’existence possible de chaque porphyrine sous plusieurs formes isomériques. La nature n’en a retenu en général que deux, appelées isomères I et III, dont la présence dans les milieux biologiques est un fait de grande importance. La transformation mutuelle de ces deux variétés isomériques nécessitant la complète dégradation et la reconstitution de leur molécule, elle est impossible dans l’organisme. Aussi chacun de ces deux isomères suit-il son chemin métabolique propre. Au cours des états pathologiques, caractérisés par les perturbations du métabolisme des porphyrines, l’accumulation prédominante soit des isomères I, soit des isomères III présente une valeur diagnostique.Si l’on se reporte à la formule chimique de la porphine et aux quatre variétés des fonctions qui peuvent remplacer les atomes d’hydrogène de la porphine, on peut aisément indiquer la structure des principales porphyrines (fig. 1):– l’uroporphyrine I : tétraacétyl-1, 3, 5, 7 tétrapropanoïque-2, 4, 6, 8 porphine;– l’uroporphyrine III : tétraacétyl-1, 3, 5, 8 tétrapropanoïque-2, 4, 6, 7 porphine;– la coproporphyrine I : tétraméthyl-1, 3, 5, 7 tétrapropanoïque-2, 4, 6, 8 porphine;– la coproporphyrine III : tétraméthyl-1, 3, 5, 8 tétrapropanoïque-2, 4, 6, 7 porphine;– la protoporphyrine : tétraméthyl-1, 3, 5, 8 divinyl-2, 4 dipropanoïque-6, 7 porphine.La protoporphyrine (porphyrine biologiquement la plus importante chez les Mammifères, donc chez l’homme) n’existe dans la nature que sous une seule forme isomérique, correspondant à l’isomère III des autres porphyrines. Combinée à un atome de fer, elle constitue l’hème des hémoprotéines (hémoglobine, myoglobine, etc.).La réduction énergique d’une porphyrine donne un produit incolore dépourvu de fluorescence, qui renferme six atomes d’hydrogène de plus que la porphyrine correspondante. Sous l’effet de l’air atmosphérique, par exemple, le produit se réoxyde en porphyrine, d’où le nom de porphyrinogène . Ainsi, les deux coproporphyrines naturelles peuvent être réduites en deux coproporphyrinogènes. Les porphyrinogènes jouent un rôle primordial au cours de la biosynthèse des porphyrines. Il existe des méthodes biochimiques relativement simples qui permettent de doser des quantités extrêmement faibles de ces diverses variétés de porphyrines dans les milieux biologiques.Biosynthèse des porphyrinesVoie de la biosynthèseDans l’organisme, les porphyrines sont d’origine endogène (formation dans les cellules). Leur biosynthèse constitue une voie très complexe, commune à toutes les cellules animales, végétales et bactériennes (fig. 2). Chez les Mammifères, les lieux principaux de la biosynthèse des porphyrines sont le foie et la moelle osseuse.Les précurseurs directs de l’hème sont deux composés très simples: l’acide succinique (constituant du cycle de Krebs) et le glycocolle (l’acide aminé le plus simple). La combinaison équimoléculaire de ces substrats conduit à la formation de l’acide 嗀-aminolévulinique. Deux molécules de cet acide se condensent en un dérivé monopyrrolique, le porphobilinogène. La cyclisation de quatre molécules de porphobilinogène donne naissance aux porphyrinogènes, précurseurs hydrogénés et non colorés des porphyrines. Des deux coproporphyrinogènes (I et III), résultant de la décarboxylation des quatre groupements acétiques des uroporphyrinogènes en groupements méthyles:
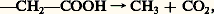 seul l’isomère III peut subir, dans les milieux biologiques, la décarboxylation et l’oxydation nécessaires à la transformation de deux résidus propanoïques en groupements vinyles caractéristiques du protoporphyrinogène et de la protoporphyrine:
seul l’isomère III peut subir, dans les milieux biologiques, la décarboxylation et l’oxydation nécessaires à la transformation de deux résidus propanoïques en groupements vinyles caractéristiques du protoporphyrinogène et de la protoporphyrine: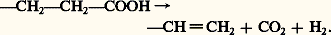 Enfin, l’incorporation d’un atome de fer bivalent dans la molécule de protoporphyrine est à l’origine de l’hème.La voie métabolique de la biosynthèse des porphyrines se complique du fait qu’à partir de l’uroporphyrinogène la décarboxylation des chaînes latérales se produit en réalité une chaîne après l’autre, et conduit à des porphyrinogènes hepta-, hexa- et pentacarboxyliques, entre l’uroporphyrinogène et le coproporphyrinogène. Ces chromogènes intermédiaires à 7, 6, 5 et 3 carboxyles n’ont pas été indiqués dans le schéma, car ils ne présentent, du fait de leurs concentrations infimes dans les milieux biologiques, qu’un intérêt physiologique ou pathologique limité.L’acide 嗀-aminolévulinique et le porphobilinogène sont, par contre, des composés très importants, car leur accumulation dans les urines caractérise certaines variétés de porphyries. En outre, le taux urinaire élevé de l’acide 嗀-aminolévulinique constitue un excellent signe biochimique pour dépister une intoxication latente par le plomb.Régulation quantitative de la biosynthèseLa régulation quantitative de la biosynthèse des porphyrines est extrêmement précise. L’organisme humain normal ne renferme que des traces de porphyrines libres . La synthèse satisfait, avec une remarquable exactitude, les besoins nécessaires à la formation des porphyrines combinées (hémoglobine, myoglobine, etc.; tabl. 1). Le mécanisme de cette régulation est encore assez mal connu. Les recherches biologiques indiquent:– une inhibition rétrograde de l’acide 嗀-aminolévulinique-synthétase par la protoporphyrine et l’hème;– la répression physiologique du gène opérateur qui tient sous sa dépendance la formation de l’acide 嗀-aminolévulinique-synthétase (cf. ENZYMES, biologie MOLÉCULAIRE). S. Granick pense que le corépresseur est l’hème. Ainsi, l’excès, même très faible, de ce dernier composé pourrait arrêter toute la chaîne des réactions qui conduit à la formation des porphyrines. La néo-formation accélérée de l’acide 嗀-aminolévulinique-synthétase et, partant, l’accumulation des porphyrines sous l’effet de certains agents toxiques s’expliqueraient par le fait que ces toxiques occuperaient, par compétition, la place même de l’hème sur l’aporépresseur, rendant celui-ci inactif. La synthèse porphyrinique serait alors libérée de son frein physiologique;– le rôle régulateur de la teneur des cellules en acide adénosine triphosphorique (ATP). De nombreuses expériences ont montré, d’une part, que la diminution en teneur des cellules en ATP, sous l’action des agents porphyrinogènes, est suivie d’une formation exagérée des porphyrines (l’ATP est donc un inhibiteur de la biosynthèse des porphyrines); d’autre part, que cet effet régulateur de l’ATP intervient avant l’action de l’acide 嗀-aminolévulinique-synthétase, donc à l’étape toute première de la porphyrinogenèse, celle qui précède la synthèse de l’acide 嗀-aminolévulinique-synthétase. Toutefois, le mécanisme biochimique exact de l’action de l’ATP dans la régulation quantitative de la porphyrinogenèse reste à établir.La baisse de la concentration intracellulaire de l’ATP au cours des porphyries expérimentales a été confirmée par plusieurs chercheurs. Le rôle régulateur de l’ATP dans la porphyrinogenèse a conduit à son emploi thérapeutique ou à l’emploi de certains précurseurs de ce nucléotide (AMP, inosine) dans le traitement des diverses variétés des porphyries humaines (A. Gajdos et coll.).Taux normaux des porphyrines libres et de leurs précurseurs chez l’hommeL’organisme humain renferme et élimine les porphyrines libres et leurs précurseurs en quantités très faibles. Les urines normales éliminent en 24 heures: environ 2 mg d’acide 嗀-aminolévulinique, 1 à 2 mg de porphobilinogène et 100 à 200 猪g de coproporphyrine avec prédominance de l’isomère III de ce pigment. Les matières fécales renferment, par gramme de poids sec, environ 10 猪g de coproporphyrine et 50 à 60 猪g de protoporphyrine. Cette dernière substance existe aussi à l’état libre, non hémoglobinique, dans les globules rouges, à un taux inférieur à 100 猪g par 100 ml. L’uroporphyrine est pratiquement absente dans les organes et les liquides biologiques normaux.2. Les porphyriesLes porphyries, affections familiales héréditaires, génétiquement déterminées, constituent un groupe de maladies comprenant plusieurs variétés. Dans la plupart des pays, dont la France, on trouve un à deux sujets atteints de porphyrie pour 100 000 habitants.Classification et fréquenceOn connaît actuellement six variétés de porphyries: porphyrie érythropoïétique ou maladie de Günther, porphyrie intermittente aiguë, porphyrie cutanée dite tardive, porphyrie mixte ou variegata , coproporphyrie héréditaire et protoporphyrie érythropoïétique.La fréquence et la gravité de ces affections sont très variables. Dans la statistique établie par nos soins, portant sur 192 cas, la répartition des diverses variétés est indiquée au tableau 2. Des répartitions similaires ont été relevées dans la plupart des pays.Étude cliniqueCes diverses porphyries présentent des tableaux cliniques caractéristiques.La porphyrie érythropoïétique , heureusement rare (environ 100 cas ont été publiés dans la littérature médicale mondiale), est la seule variété dont l’évolution soit toujours grave. Cette gravité provient, chez un individu, d’une part d’une grande photosensibilité provoquant dès la naissance des éruptions cutanées mutilantes au visage et sur les mains, d’autre part des crises hémolytiques déterminant des périodes d’anémie parfois très sévère. Les sujets atteints dépassent rarement l’âge de vingt ans.La porphyrie intermittente aiguë , variété la plus fréquente, se manifeste cliniquement en général après la puberté. Elle est caractérisée par trois syndromes apparaissant isolément ou simultanément: abdominal (douleurs aiguës, vomissements, constipation), neurologique (paralysie des membres, paralysie respiratoire souvent mortelle), psychique (allant des perturbations mineures jusqu’aux psychoses graves). Un fait particulièrement important est le déclenchement de ces diverses manifestations cliniques par certains médicaments, les barbituriques (Gardénal, ou phénobarbital, etc.) étant les plus redoutables. Quelques comprimés de Gardénal suffisent parfois pour provoquer un syndrome neurologique mortel. Or, si le diagnostic correct n’est pas établi, la prescription des barbituriques est très fréquente, soit à cause de l’état nerveux habituel de ces malades, soit à la suite des interventions chirurgicales, d’ailleurs absolument inutiles, que semble motiver une crise douloureuse abdominale aiguë. Ces erreurs thérapeutiques sont d’autant plus regrettables que la porphyrie intermittente aiguë est une maladie généralement bénigne. Même à l’heure actuelle, où les porphyries commencent à être mieux connues, il n’est pas exagéré de dire que le plus grand danger pour les malades est constitué par les erreurs que peuvent commettre le médecin ou le pharmacien. L’extraordinaire sensibilité aux barbituriques des sujets porteurs de la tare de la porphyrie intermittente aiguë rend obligatoire, dans chaque cas, une enquête biochimique pour déceler les autres membres de la famille éventuellement atteints de la maladie. Comme celle-ci est héritée suivant le mode mendélien dominant, la tare est transmise à un enfant sur deux.La porphyrie cutanée (dite tardive, bien qu’elle puisse s’observer même chez l’enfant) se traduit par des poussées d’éruptions bulleuses (dues à une grande photosensibilité cutanée) localisées aux parties découvertes de la peau. L’administration d’hormones stéroïdes, de la griséofulvine et la consommation d’alcool aggravent la photosensibilité, mais les barbituriques sont relativement bien supportés. La maladie, en général bénigne, peut se compliquer de diabète ou de cirrhose hépatique.La porphyrie variegata réunit chez le même sujet, ou chez divers membres d’une même famille, les manifestations cliniques et biochimiques de la porphyrie intermittente aiguë, et aussi de la porphyrie cutanée. La porphyrie variegata est une maladie peu répandue, sauf en Afrique du Sud, où plusieurs centaines de cas ont été reconnus. Dans ce pays tous les sujets atteints sont les descendants d’une même aïeule émigrée au Cap au XVIIe siècle. On avait pu identifier plusieurs milliers de personnes vivantes appartenant à cette famille: 50 p. 100 des descendants étaient porteurs de la tare. Ce fait illustre bien le caractère spontanément bénin de cette porphyrie, en l’absence de prescription de médicaments nocifs, surtout des barbituriques.La coproporphyrie héréditaire est très rare. Elle peut cliniquement rester tout à fait latente ou se traduire par la symptomatologie de la porphyrie intermittente aiguë.La protoporphyrie érythropoïétique est caractérisée, sur le plan clinique, par la seule urticaire solaire.Comme la nature héréditaire des porphyries l’a laissé prévoir, ces affections sont provoquées par la déficience des enzymes intervenant aux diverses étapes de la biosynthèse des porphyrines. On peut s’étonner de la découverte tardive de ces déficiences enzymatiques. La cause en est sans doute l’importance erronée attribuée pendant longtemps au rôle de l’acide 嗀-aminolévulinique-synthétase, dont l’activité accrue a été considérée, par certains auteurs, comme la cause des porphyries.Ce n’est qu’au cours des années soixante qu’on a démontré une déficience enzymatique spécifique pour chaque variété de porphyries. Nous ne pouvons ici que réunir dans un tableau (tabl. 3) les résultats de ces recherches.L’établissement de la nature enzymopathique des diverses porphyries présente une grande importance pratique. Il permet, par le dosage de l’activité de l’enzyme déficiente, de diagnostiquer la porphyrie biochimiquement et cliniquement latente. Grâce à ce diagnostic précoce par l’enquête familiale enzymologique, on peut écarter les facteurs, le plus souvent médicamenteux, susceptibles de déclencher les manifestations cliniques, parfois dramatiques, de la maladie.La déficience enzymatique explique les troubles métaboliques des porphyrines qui caractérisent chaque variété de porphyries.La nature enzymopathique précise des porphyries ouvre la voie, sans doute encore longue, conduisant au traitement étiologique de ces affections.
Enfin, l’incorporation d’un atome de fer bivalent dans la molécule de protoporphyrine est à l’origine de l’hème.La voie métabolique de la biosynthèse des porphyrines se complique du fait qu’à partir de l’uroporphyrinogène la décarboxylation des chaînes latérales se produit en réalité une chaîne après l’autre, et conduit à des porphyrinogènes hepta-, hexa- et pentacarboxyliques, entre l’uroporphyrinogène et le coproporphyrinogène. Ces chromogènes intermédiaires à 7, 6, 5 et 3 carboxyles n’ont pas été indiqués dans le schéma, car ils ne présentent, du fait de leurs concentrations infimes dans les milieux biologiques, qu’un intérêt physiologique ou pathologique limité.L’acide 嗀-aminolévulinique et le porphobilinogène sont, par contre, des composés très importants, car leur accumulation dans les urines caractérise certaines variétés de porphyries. En outre, le taux urinaire élevé de l’acide 嗀-aminolévulinique constitue un excellent signe biochimique pour dépister une intoxication latente par le plomb.Régulation quantitative de la biosynthèseLa régulation quantitative de la biosynthèse des porphyrines est extrêmement précise. L’organisme humain normal ne renferme que des traces de porphyrines libres . La synthèse satisfait, avec une remarquable exactitude, les besoins nécessaires à la formation des porphyrines combinées (hémoglobine, myoglobine, etc.; tabl. 1). Le mécanisme de cette régulation est encore assez mal connu. Les recherches biologiques indiquent:– une inhibition rétrograde de l’acide 嗀-aminolévulinique-synthétase par la protoporphyrine et l’hème;– la répression physiologique du gène opérateur qui tient sous sa dépendance la formation de l’acide 嗀-aminolévulinique-synthétase (cf. ENZYMES, biologie MOLÉCULAIRE). S. Granick pense que le corépresseur est l’hème. Ainsi, l’excès, même très faible, de ce dernier composé pourrait arrêter toute la chaîne des réactions qui conduit à la formation des porphyrines. La néo-formation accélérée de l’acide 嗀-aminolévulinique-synthétase et, partant, l’accumulation des porphyrines sous l’effet de certains agents toxiques s’expliqueraient par le fait que ces toxiques occuperaient, par compétition, la place même de l’hème sur l’aporépresseur, rendant celui-ci inactif. La synthèse porphyrinique serait alors libérée de son frein physiologique;– le rôle régulateur de la teneur des cellules en acide adénosine triphosphorique (ATP). De nombreuses expériences ont montré, d’une part, que la diminution en teneur des cellules en ATP, sous l’action des agents porphyrinogènes, est suivie d’une formation exagérée des porphyrines (l’ATP est donc un inhibiteur de la biosynthèse des porphyrines); d’autre part, que cet effet régulateur de l’ATP intervient avant l’action de l’acide 嗀-aminolévulinique-synthétase, donc à l’étape toute première de la porphyrinogenèse, celle qui précède la synthèse de l’acide 嗀-aminolévulinique-synthétase. Toutefois, le mécanisme biochimique exact de l’action de l’ATP dans la régulation quantitative de la porphyrinogenèse reste à établir.La baisse de la concentration intracellulaire de l’ATP au cours des porphyries expérimentales a été confirmée par plusieurs chercheurs. Le rôle régulateur de l’ATP dans la porphyrinogenèse a conduit à son emploi thérapeutique ou à l’emploi de certains précurseurs de ce nucléotide (AMP, inosine) dans le traitement des diverses variétés des porphyries humaines (A. Gajdos et coll.).Taux normaux des porphyrines libres et de leurs précurseurs chez l’hommeL’organisme humain renferme et élimine les porphyrines libres et leurs précurseurs en quantités très faibles. Les urines normales éliminent en 24 heures: environ 2 mg d’acide 嗀-aminolévulinique, 1 à 2 mg de porphobilinogène et 100 à 200 猪g de coproporphyrine avec prédominance de l’isomère III de ce pigment. Les matières fécales renferment, par gramme de poids sec, environ 10 猪g de coproporphyrine et 50 à 60 猪g de protoporphyrine. Cette dernière substance existe aussi à l’état libre, non hémoglobinique, dans les globules rouges, à un taux inférieur à 100 猪g par 100 ml. L’uroporphyrine est pratiquement absente dans les organes et les liquides biologiques normaux.2. Les porphyriesLes porphyries, affections familiales héréditaires, génétiquement déterminées, constituent un groupe de maladies comprenant plusieurs variétés. Dans la plupart des pays, dont la France, on trouve un à deux sujets atteints de porphyrie pour 100 000 habitants.Classification et fréquenceOn connaît actuellement six variétés de porphyries: porphyrie érythropoïétique ou maladie de Günther, porphyrie intermittente aiguë, porphyrie cutanée dite tardive, porphyrie mixte ou variegata , coproporphyrie héréditaire et protoporphyrie érythropoïétique.La fréquence et la gravité de ces affections sont très variables. Dans la statistique établie par nos soins, portant sur 192 cas, la répartition des diverses variétés est indiquée au tableau 2. Des répartitions similaires ont été relevées dans la plupart des pays.Étude cliniqueCes diverses porphyries présentent des tableaux cliniques caractéristiques.La porphyrie érythropoïétique , heureusement rare (environ 100 cas ont été publiés dans la littérature médicale mondiale), est la seule variété dont l’évolution soit toujours grave. Cette gravité provient, chez un individu, d’une part d’une grande photosensibilité provoquant dès la naissance des éruptions cutanées mutilantes au visage et sur les mains, d’autre part des crises hémolytiques déterminant des périodes d’anémie parfois très sévère. Les sujets atteints dépassent rarement l’âge de vingt ans.La porphyrie intermittente aiguë , variété la plus fréquente, se manifeste cliniquement en général après la puberté. Elle est caractérisée par trois syndromes apparaissant isolément ou simultanément: abdominal (douleurs aiguës, vomissements, constipation), neurologique (paralysie des membres, paralysie respiratoire souvent mortelle), psychique (allant des perturbations mineures jusqu’aux psychoses graves). Un fait particulièrement important est le déclenchement de ces diverses manifestations cliniques par certains médicaments, les barbituriques (Gardénal, ou phénobarbital, etc.) étant les plus redoutables. Quelques comprimés de Gardénal suffisent parfois pour provoquer un syndrome neurologique mortel. Or, si le diagnostic correct n’est pas établi, la prescription des barbituriques est très fréquente, soit à cause de l’état nerveux habituel de ces malades, soit à la suite des interventions chirurgicales, d’ailleurs absolument inutiles, que semble motiver une crise douloureuse abdominale aiguë. Ces erreurs thérapeutiques sont d’autant plus regrettables que la porphyrie intermittente aiguë est une maladie généralement bénigne. Même à l’heure actuelle, où les porphyries commencent à être mieux connues, il n’est pas exagéré de dire que le plus grand danger pour les malades est constitué par les erreurs que peuvent commettre le médecin ou le pharmacien. L’extraordinaire sensibilité aux barbituriques des sujets porteurs de la tare de la porphyrie intermittente aiguë rend obligatoire, dans chaque cas, une enquête biochimique pour déceler les autres membres de la famille éventuellement atteints de la maladie. Comme celle-ci est héritée suivant le mode mendélien dominant, la tare est transmise à un enfant sur deux.La porphyrie cutanée (dite tardive, bien qu’elle puisse s’observer même chez l’enfant) se traduit par des poussées d’éruptions bulleuses (dues à une grande photosensibilité cutanée) localisées aux parties découvertes de la peau. L’administration d’hormones stéroïdes, de la griséofulvine et la consommation d’alcool aggravent la photosensibilité, mais les barbituriques sont relativement bien supportés. La maladie, en général bénigne, peut se compliquer de diabète ou de cirrhose hépatique.La porphyrie variegata réunit chez le même sujet, ou chez divers membres d’une même famille, les manifestations cliniques et biochimiques de la porphyrie intermittente aiguë, et aussi de la porphyrie cutanée. La porphyrie variegata est une maladie peu répandue, sauf en Afrique du Sud, où plusieurs centaines de cas ont été reconnus. Dans ce pays tous les sujets atteints sont les descendants d’une même aïeule émigrée au Cap au XVIIe siècle. On avait pu identifier plusieurs milliers de personnes vivantes appartenant à cette famille: 50 p. 100 des descendants étaient porteurs de la tare. Ce fait illustre bien le caractère spontanément bénin de cette porphyrie, en l’absence de prescription de médicaments nocifs, surtout des barbituriques.La coproporphyrie héréditaire est très rare. Elle peut cliniquement rester tout à fait latente ou se traduire par la symptomatologie de la porphyrie intermittente aiguë.La protoporphyrie érythropoïétique est caractérisée, sur le plan clinique, par la seule urticaire solaire.Comme la nature héréditaire des porphyries l’a laissé prévoir, ces affections sont provoquées par la déficience des enzymes intervenant aux diverses étapes de la biosynthèse des porphyrines. On peut s’étonner de la découverte tardive de ces déficiences enzymatiques. La cause en est sans doute l’importance erronée attribuée pendant longtemps au rôle de l’acide 嗀-aminolévulinique-synthétase, dont l’activité accrue a été considérée, par certains auteurs, comme la cause des porphyries.Ce n’est qu’au cours des années soixante qu’on a démontré une déficience enzymatique spécifique pour chaque variété de porphyries. Nous ne pouvons ici que réunir dans un tableau (tabl. 3) les résultats de ces recherches.L’établissement de la nature enzymopathique des diverses porphyries présente une grande importance pratique. Il permet, par le dosage de l’activité de l’enzyme déficiente, de diagnostiquer la porphyrie biochimiquement et cliniquement latente. Grâce à ce diagnostic précoce par l’enquête familiale enzymologique, on peut écarter les facteurs, le plus souvent médicamenteux, susceptibles de déclencher les manifestations cliniques, parfois dramatiques, de la maladie.La déficience enzymatique explique les troubles métaboliques des porphyrines qui caractérisent chaque variété de porphyries.La nature enzymopathique précise des porphyries ouvre la voie, sans doute encore longue, conduisant au traitement étiologique de ces affections.
Encyclopédie Universelle. 2012.
